【Cell】华大徐讯团队:时空组学在生物学和医学的应用
| 导读 | 这篇综述,提供了空间组学如何推进科学界对遗传信息转化为细胞异质性和组织结构,及其随时间动态变化的理解的最新概述。 |
2024年8月22日, 华大生命科学研究院徐讯团队在期刊《Cell》上发表了题为“Spatiotemporal omics for biology and medicine”的研究论文。这篇综述强调,科学界通过利用空间组学技术,可以发现与器官功能、胚胎发生、物种进化和疾病发病机制有关的各种生物学现象。
https://www.cell.com/cell/fulltext/S0092-8674(24)00834-1#%20
研究背景
01
整个20世纪分子生物学的进步,特别是中心教条的制定,揭示了人类的遗传信息是如何被转录成信使RNA(mRNA),然后被翻译成蛋白质的,揭示了基因遗传、进化、适应和功能表达背后的核心过程。在这些基本原则的基础上,人类基因组计划(HGP)开始了一项任务,即识别和绘制构成人类遗传密码的30亿个DNA碱基对和25,000个基因,开创了研究人类的遗传信息如何决定生物学功能的新时代。HGP带来的主要挑战之一,是理解基因组序列向复杂生物系统的翻译。例如,基于广泛群体的大规模基因组分析,1,000基因组计划和全基因组关联研究(GWASs),发现了许多与人类表型和疾病相关的变异。然而,关于这些变异如何影响特定器官或细胞的功能,仍然存在一个关键问题。要应对这些挑战,就必须全面了解分子水平的序列信息,如何转化为构成功能性生物系统的通信和相互作用细胞网络中的单个细胞。这包括:(1)定性 — 通过调控基因表达产生的细胞类型的多样性;(2)定量 — 每种细胞类型的计数、比例和密度;(3)空间 — 每种细胞类型的空间布局及其相互作用和细胞生态系统;(4)时间 — 细胞类型和状态变化的具体时间;(5)方向 — 每种细胞类型可能经历的潜在转化路径。
2009年,单细胞测序技术的出现,及其在通量、成本和多模态能力方面的快速发展,为理解组织内细胞异质性,提供了前所未有的工具。目前,单细胞组学能够定义多个维度的细胞类型和状态,包括基因组学、转录组学、表观基因组学和蛋白质组学谱。然而,要获得所有组织驻留细胞类型和细胞状态的良好表达,仍然具有挑战性。特别是,稀有细胞的捕获,需要大量的分析细胞(无偏倚)或细胞选择(偏倚)方法,才能达到比较细胞类型之间的统计功效水平。此外,组织内细胞的特定空间环境,形成具有不同功能的器官,带来了额外的复杂性。空间组学技术的最新发展,通过提供解决方案,来获取组织中的高内涵组学数据,同时保留空间定位信息,从而解决了这些限制。空间组学技术能够全面绘制细胞组成、定位、细胞间相互作用和细胞生态系统的空间动态图。
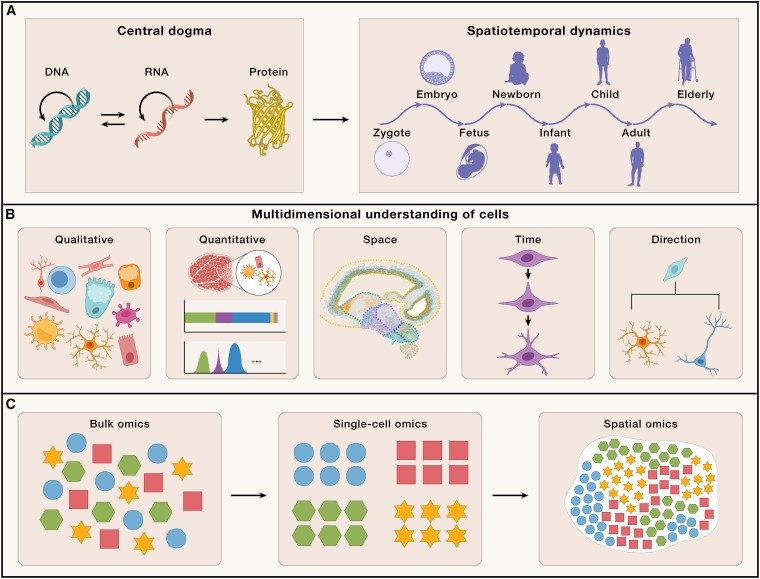
细胞的多维测量
研究进展
02
空间组学的生物学和临床应用
生物系统本质上是空间性的,具有不同的细胞微环境和组织结构,在确定基因表达模式和细胞功能方面,起着关键作用。捕捉基因表达的空间维度,对于获得细胞生态系统的完整图景,至关重要。空间组学技术能够将分子信号精确映射到组织内的特定位置,从而为细胞如何与其周围环境相互作用,并促进组织的整体功能,提供了宝贵的见解。通过整合空间和时间背景,研究人员现在可以揭示各种生物过程中细胞行为、组织和分子调控之间的复杂关系,从而推进科学界对器官功能、发育生物学、物种进化、疾病机制和治疗干预的理解。
解读疾病发病和进展的机制
基于群体的基因组测序研究,确定了许多与疾病相关的基因组变异。然而,绘制这些基因组位点的确切细胞或组织转录活性,已被证明是一个挑战,阻碍了对遗传变异对生物学功能影响的理解。批量转录组学、表观基因组学或蛋白质组学方法,极大地促进了科学界对与疾病相关的基因表达和调控的理解。这些方法有助于发现异常情况,并促进确定疾病检测或治疗的其他靶点。然而,需要注意的是,这些方法很难识别与疾病发展相关的特定细胞类型和组织环境中的改变。单细胞测序可对包括癌症在内的各种疾病和患病状况,进行全面深入的分析,识别多种与疾病相关的细胞类型及其改变的微环境。然而,单细胞测序无法实现病变结构特征和微环境中相互作用所需的详细分辨率。
空间组学可以更详细地了解组织和微环境中,与疾病相关的遗传变异,以及表观基因组和转录组学改变。一方面,它提供了与缺氧、上皮-间充质转化或炎症等特征相关的基因和信号通路的分布,这些特征与其原位病理特征相关。在癌症中,识别肿瘤切片上的不同突变亚克隆,能够研究与组织学进展相关的空间模式,有助于识别导致转移的肿瘤亚群的分子特征。其他研究结合基因和蛋白质表达的空间分布,探索了胶质母细胞瘤肿瘤异质性与空间组织之间的关联,揭示了肿瘤进展和治疗耐药性的驱动因素。空间转录组学还可以研究肿瘤微环境中的细胞间相互作用,包括肿瘤、基质和免疫细胞之间的关系。在肺癌患者的肿瘤巢中,发现了癌症相关成纤维细胞(CAF),肿瘤边界富集的MYH11+αSMA+和FAP+αSMA+CAF与显著的纤维组织沉积相关,影响T细胞浸润,并可能影响免疫治疗反应。此外,浸润性肝癌通过空间转录组学进行了表征,揭示了受损肝细胞募集巨噬细胞,是肝癌进展的关键因素。分析空间结构(如三级淋巴样结构)内的细胞相互作用也为治疗反应,提供了见解或抵抗。
除癌症研究外,空间组学在慢性病和传染病研究中,也至关重要。例如,淀粉样斑块细胞生态位中的小胶质细胞和星形胶质细胞之间的相互作用,可能导致阿尔茨海默病的发展。在COVID-19等传染病中,空间组学提供了对感染过程中分子过程的见解,为了解病毒对不同组织的影响,提供了宝贵的空间信息。通过分析细胞的空间位置和基因表达模式,研究人员提出SARS-CoV-2可能通过血管紧张素转换酶2(ACE2)感染嗅觉上皮中的支撑细胞,避免了嗅觉感觉神经元的直接感染。COVID-19患者的嗅觉功能丧失,可能是由于感染的支撑细胞中的转录组失调,导致对嗅觉感觉神经元的支持不足,从而损害了它们的功能。
总而言之,空间组学技术的出现使得在分子、细胞和组织水平上,同时研究疾病成为可能。整合这些信息层,将增强科学界对疾病进展机制的理解,从而加速新的临床诊断和干预措施的开发。然而,在将空间组学应用于临床研究时,仍然存在一些挑战。其中包括:(1)多组学信息 — 全面理解遗传变异的影响,有效整合遗传疾病中各种组学数据,如基因组变异、表观遗传信号、具有空间多组学特征的翻译后修饰等,仍然是一个挑战;(2)监测时间信息 — 疾病的发生和发展是一个动态和演变的过程,因此,疾病发生、进展和治疗过程中的时间信息,对于全面理解疾病和制定相应的治疗策略,至关重要;(3)病原体检测 — 在传染病中,病原体检测仍然是一个重大的技术挑战,因为很难同时检测组织内病原体和宿主的分子特征。
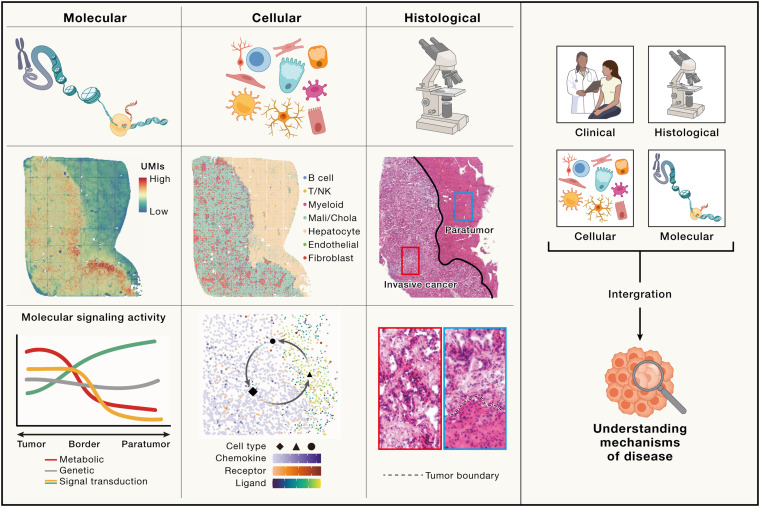
空间组学在揭示疾病发病机制中的作用
空间组学的临床应用:从实验室到床边
空间组学在解码肿瘤微环境和促进理解疾病的发生和进展方面具有重要贡献,而这正是精准医学的基础。空间组学技术可以将显现的组织结构与高分辨率的分子特征相关联,并且有可能在临床环境中使用空间分子谱作为诊断工具,从而改善需要个性化复杂治疗策略的具有高度异质性的疾病的分层。然而,此类强力工具的临床可及性,仍受到稳定性、可重复性、合理性、实用性、高成本和可及性的限制。
免疫疗法的最新进展,包括免疫检查点抑制剂、基于细胞的疗法和mRNA疫苗,已成功满足监管要求,显著提高了许多晚期癌症的治疗选择和结果。然而,由于肿瘤微环境中复杂的感知和反应过程,这一突破给开发有效的分层方法,带来了巨大的挑战。空间组学检测在识别具有高诊断和预后准确性的生物标志物方面,发挥了关键作用,从而为单一疗法和联合免疫疗法策略,提供信息。尽管取得了这些进展,但空间组学仍面临一些局限性,例如,成本高、周转时间长、不同平台之间的不一致,以及对复杂生物信息学的需求,这些共同限制了其临床应用。
空间组学分析还提供了一个有前途的平台,可以通过原位空间信息将组织和细胞的形态特征,与基因表达相关联。这种方法使人工智能算法的训练成为可能,将H&E特性与细胞状态、细胞间通信和其他基于基因表达谱的生物活动联系起来。鉴于H&E染色是病理学中最普遍的方式,在空间分辨的转录组数据上训练的AI分析,可以整合到临床实践中。这种集成有望降低成本和数据存储要求,并提高准确性。然而,这些技术的转化应用面临障碍,包括缺乏详细的方案和病理学专家的评估,数据质量控制方面的挑战,以及缺乏具有足够样本量的前瞻性、随机、多中心试验,来客观评估其对病理学家和患者的影响。
除了治疗决策外,另一个临床挑战,是高复杂性疾病的诊断。高度异质性疾病(如未分化肿瘤和原发性不明的癌症)的常规诊断程序,需要超过12个IHC染色和预留切片用于基因组亚型,仍然导致错误分类的高风险。据统计,在首次诊断和专家第二意见之间,19.7%的淋巴瘤患者的分类诊断发生了变化,对患者护理产生了负面影响。基因或蛋白质分析的空间多路复用,通过将多个生物标志物及其共同定位,整合在一个切片中,来克服这些困难。
最近的研究表明,与单路方法相比,多路复用方法产生的诊断或预后,与患者结果更密切相关。例如,对不同伴随检测之间的预测能力的系统评价表明,通过多路免疫荧光成像进行空间表型分析,在预测癌症患者PD-1治疗结果方面,提供了最高的准确性。通过成像质谱流式术检测增殖的CD8+TCF1+T细胞和MHCII+癌细胞群,可以预测三阴性乳腺癌的免疫治疗反应。然而,空间多路复用技术的缺陷,例如,多路免疫荧光(mIF)中特定波长捕获的信息不透明,以及靶点有限,导致临床实用性低下。基于测序的多路复用方法可以提供一种潜在的解决方案,该方法可以同时进行基因检测和蛋白质标记物的染色,分辨率接近单细胞。此外,转录组学和蛋白质组学分析的同时检测,可实现定量性能和空间分析。以等待基于穿刺活检的治疗决策的肺癌患者为例,Stereo-CITE-seq可以确定TTF1、napsin、p63和细胞角蛋白的常规诊断,并确定PD-L1、PD-1、CD68、CD45、CD8和CD3等其他生物标志物,以确定免疫检查点治疗的适用性,指导最优治疗策略。
在临床实验室中,空间组学方法需要使用标准化和防故障的协议、自我解释和可重复的结果,以及数字病理学的工作流程。验证检测的伦理、法律和社会影响,对于证明空间组学的有效性和稳健性,至关重要。合理的仪器要求、较低的成本、减少人力,以及对经验丰富的专家的需求最小(或不需要),可以改善临床环境中,空间组学的可及性,包括在资源匮乏的研究中心。总之,空间组学分析可以开启一个解释临床相关信息的新时代,以改善基于综合知识的患者护理结果。
大规模时空组学研究的全球努力
生命过程的复杂性和海量的数据,使得大规模、跨学科的研究,成为一种普遍的趋势。继HGP之后,大规模的基因组研究,已经从基因组解码(例如,国际HapMap、1,000基因组计划和英国生物样本库)到功能基因组学分析(例如,DNA元素百科全书[ENCODE],国际人类表观基因组联盟(IHEC),基因型-组织表达[GTEx]和人类蛋白质图谱 [HPA]),并最终进入细胞基因组学分析时代。
人类细胞图谱(HCA)是第一个国际合作研究联盟,旨在绘制从发育到成年和老年的身体所有细胞类型。迄今为止,全球HCA社区已经分析了来自近10,000个体的数千万个细胞。在此基础上,HuBMAP有了旨在整合细胞图谱数据,构建详细而全面的人体组织生物分子图谱。此外,时空组学联盟(STOC)专注于从时空动力学理解生物学问题,旨在通过大规模空间分辨的多组学分析,加速科学界对细胞复杂性和组织尺度上发育、生理学和疾病相互作用的理解。
在各个领域,大规模的合作研究突出,特别是在脑和肿瘤研究方面。在脑科学方面,BRAIN倡议细胞普查网络(BICCN),这是一项显著的成功,旨在建立参考脑细胞图谱,为研究大脑功能和疾病,提供分子和解剖学基础。各种国家脑计划,包括欧盟的人脑计划(HBP),中国脑计划,以及日本的Brain/MINDS。在肿瘤研究中,人类肿瘤图谱网络,旨在以单细胞分辨率,绘制肿瘤跨空间和时间的转变,增强科学界对癌症生物学的理解,并有可能改善癌症检测、预防和治疗发现,从而对癌症患者进行精准医学治疗。
单细胞和空间组学在通量、成本和可及性方面正在迅速发展,使全球科学合作成为可能。然而,实现更高效的团队协作,以最大限度地提高基因组大数据生产和分析的价值,仍然具有挑战性。进一步的考虑可能包括:(1)成立技术和算法开发的协作小组,涉及跨学科、跨部门的伙伴关系,这需要来自不同背景的团队联合起来;(2)创建全球多中心组学平台,确保不同团队之间的一致性;(三)成立数据协作组,推动多中心数据共享、分析方法共享、数据库共享;(4)制定技术、平台和数据标准,以实现团队之间的协调。
研究结论
03
空间组学技术的出现和快速发展,加上测序和单细胞组学的进步,将使科学界能够在时间和空间维度上,以细胞分辨率创建人体的“谷歌地图”。这将增强科学界对生物过程背后的细胞和分子基础的理解。同时,人工智能和计算生物学的快速发展,将显著推动细胞图谱数据、影像学和临床表型数据与算法的整合,极大地推动疾病诊断、治疗和预后的方法化,加速精准医疗的临床应用。
参考资料:
1.CRICK F.
Central Dogma of Molecular Biology.
Nature. 1970; 227: 561-563
2.Collins F.S.Green E.D.Guttmacher A.E.Guyer M.S.
US National Human Genome Research Institute
A vision for the future of genomics research.
Nature. 2003; 422: 835-847
 腾讯登录
腾讯登录






还没有人评论,赶快抢个沙发