协同抑制乳腺癌生长!天津医科大学合作发文:乳腺癌精准治疗潜在方案
| 导读 | 乳腺癌是发病率最高、种类最繁多的恶性肿瘤之一,随着全球病例的增加,对能够提供个体对化疗药物敏感性的生物标志物的需求愈加迫切。 |
11月16日,天津医科大学与天津市肿瘤防治重点实验室研究人员合作在期刊《Cell Death&Disease》上发表了研究论文,题为“FATS inhibits the Wnt pathway and induces apoptosis through degradation of MYH9 and enhances sensitivity to paclitaxel in breast cancer”, 本研究表明,FATS显著增强了紫杉醇对乳腺癌细胞迁移、生长和存活的抑制作用。相互作用筛选显示,FATS与MYH9相互作用,通过泛素-蛋白酶体途径促进MYH9的降解,从而抑制Wnt信号通路。通过过表达FATS和MYH9,研究人员证明FATS通过降解MYH9来下调Wnt通路,增强了紫杉醇诱导的乳腺癌细胞凋亡。在小鼠异种移植模型中,研究人员还证明FATS在体内显著增强了乳腺癌细胞对紫杉醇的化疗敏感性。这项研究揭示了FATS通过与MYH9相互作用来抑制Wnt/β-连环蛋白信号通路并诱导细胞凋亡的新机制,从而增强了乳腺癌细胞对紫杉醇化疗的敏感性。研究结果还提出了预测乳腺癌对含紫杉醇的新辅助化疗敏感性的新型生物标志物。最后,研究人员提供了体内证据,证明新型Wnt信号通路抑制剂IWR-1与紫杉醇的联合疗法能协同抑制乳腺癌生长,为将来使用这种药物组合的临床试验奠定了基础。因此,这些结果为未来更精确治疗乳腺癌患者提供了多种潜在解决方案。

https://www.nature.com/articles/s41419-024-07164-w
背景信息
01
乳腺癌是女性中最常见的恶性肿瘤,对全球女性的健康构成严重威胁。尽管近年来在诊断和治疗方面取得了显著进展,但乳腺癌的发病机制仍复杂多样,个体间的治疗效果各不相同。一些患者对一线化疗药物产生耐药性的问题越来越普遍。因此,识别预测药物敏感性的生物标志物,以便为患有乳腺癌的个体提供精确治疗,变得越来越重要。
紫杉醇是治疗乳腺癌的成熟化疗药物,通常作为新辅助治疗的一线药物使用。然而,有些患者对紫杉醇治疗没有反应或无法通过新辅助化疗达到完全缓解。对于对紫杉醇不敏感的患者,治疗不仅无法达到预期的治疗效果,还可能延迟更有效的治疗,并因该药物的多种副作用而造成不必要的二次伤害。因此,通过检测特定的生物标志物来筛查患者对紫杉醇的敏感性,对于为乳腺癌患者实现有效且精确的治疗至关重要。
FATS基因是典型的含有丰富AT重复序列的内含子和表达调控区域的脆弱位点基因。FATS基因定位于10q26.2,由研究小组首次发现,是与DNA损伤诱导肿瘤相关的肿瘤抑制因子。荧光原位杂交(FISH)实验证实FATS位于脆性位点FRA10F。不仅在乳腺癌、卵巢癌和肺癌患者的DNA中未检测到FATS基因,而且与正常细胞和非肿瘤组织相比,许多癌细胞和肿瘤组织中FATS mRNA的表达量减少甚至缺失。此外,共转染FATS表达载体的细胞在体外和体内均显示出显著的抗肿瘤活性。研究人员在理解FATS基因抑制肿瘤发生的机制方面取得了重要进展。
FATS的表达与乳腺癌新辅助紫杉醇治疗的预后有关
02
基于从乳腺穿刺活检组织中获得的病理组织的免疫组织化学(IHC)评分,将接受辅助化疗的108例乳腺癌患者分为两组:高FATS表达组和低FATS表达组。如图1A所示,展示了FATS IHC染色的代表性图像。研究发现,FATS高表达组患者中,58.5%的患者术后病理完全缓解(pCR),占总pCR率的69%。相比之下,只有16.4%的FATS低表达组患者术后达到pCR,占总pCR率的31%。研究还显示了接受含紫杉醇辅助治疗的乳腺癌患者中pCR与临床病理特征的相关性。与以往文献一致,发现ki67的变化(p=0.006)、ypTNM分期(p<0.001)和AJCC分期(p<0.001)与达到pCR显著相关。研究人员观察到高FATS表达与雄激素受体表达增加(p=0.019)、肿瘤浸润淋巴细胞(p=0.029)和ypTNM分期(p<0.05)相关。AR和TIL对新辅助化疗的pCR的影响尚不明确。因此,本研究未研究FATS是否影响这些因素以影响pCR。然而,研究实验发现,高FATS水平与乳腺癌紫杉醇新辅助化疗后的术后pCR呈正相关(p<0.001)。这表明FATS可以作为预测乳腺癌对紫杉醇新辅助化疗敏感性的生物标志物。
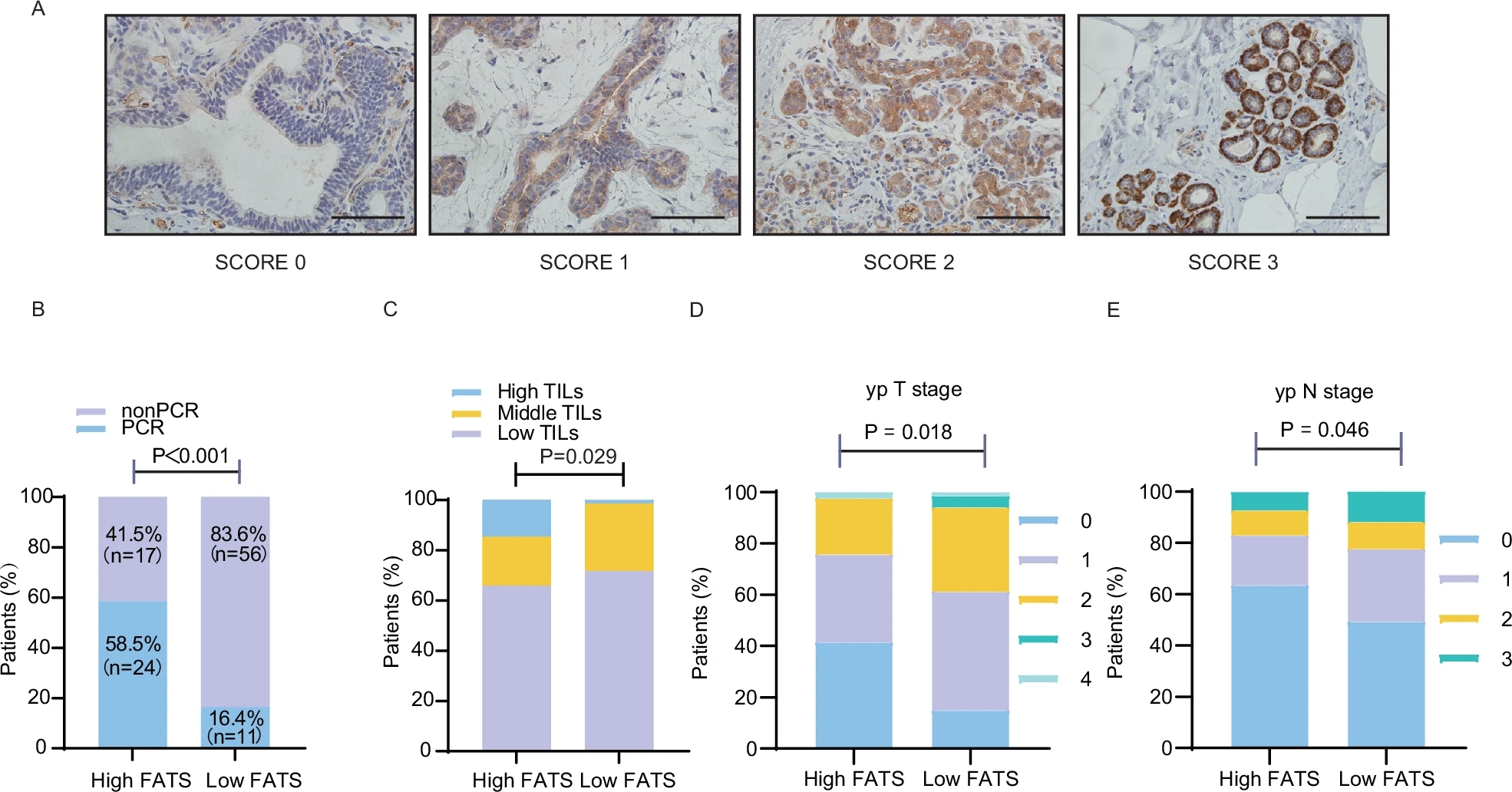
图1:临床病理学数据表明,FATS表达与乳腺癌对紫杉醇辅助化疗的敏感性有关
FATS过表达和Wnt通路抑制剂IWR-1在体内均可改善乳腺癌紫杉醇化疗敏感性
03
为了研究FATS是否能增强紫杉醇在体内的化疗敏感性,研究人员建立了小鼠乳腺癌肿瘤模型。FATS过表达和紫杉醇联合治疗组(FATS+TAXOL)与对照组(NC+TAXOL)相比,肿瘤生长速度明显减慢,晚期肿瘤有缩小趋势。FATS+TAXOL组在四个组中是肿瘤体积和肿瘤重量最小的。这些观察结果可能证实,FATS在体内与紫杉醇协同作用杀死乳腺癌细胞,与体外实验结果一致。随后,研究人员旨在通过降解MYH9来确认FATS在体内增强乳腺癌对紫杉醇的敏感性。研究人员用紫杉醇治疗了三组小鼠乳腺癌肿瘤模型:第一组未过表达FATS,第二组过表达了FATS,第三组过表达了FATS和MYH9。第三组的肿瘤明显大于第二组。体内拯救实验表明,过表达MYH9可降低FATS过表达导致的紫杉醇化疗敏感性增强,这与体外细胞实验结果一致。两例动物实验的免疫组织化学结果显示,在FATS过表达组中,MYH9水平显著降低,Wnt信号通路在与紫杉醇联合使用时受到明显抑制。此外,FATS引起的Wnt通路的抑制可通过过表达MYH9得到逆转。动物实验的免疫组织化学分析结果与细胞实验的结果一致。
研究人员已经证明FATS可以通过下调β-连环蛋白来抑制Wnt信号通路,从而增强紫杉醇的敏感性。因此,研究人员在乳腺癌小鼠模型中使用Wnt信号通路抑制剂IWR-1与紫杉醇联合治疗。研究人员发现两种药物的联合使用导致肿瘤生长、体积和重量均小于单独使用紫杉醇或IWR-1的组。这表明,IWR-1可以在体内增强紫杉醇的抗肿瘤作用。(转化医学网360zhyx.com)
【参考资料】
https://www.nature.com/articles/s41419-024-07164-w
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录








还没有人评论,赶快抢个沙发