肝癌转移新机制!武汉科技大学合作发文:转移性肝癌治疗的潜在靶点
| 导读 | TRIM蛋白家族已被证明在多种肿瘤的发生和发展中发挥重要作用。然而,TRIM47在肝细胞癌(HCC)中的生物学功能及其调控机制尚不清楚。 |
11月20日,武汉科技大学与湖北文理学院研究人员合作共同在期刊《Cell Death Discovery》上发表了研究论文,题为“Arginine methylation-dependent TRIM47 stability mediated by CARM1 promotes the metastasis of hepatocellular carcinoma”,本研究中,研究人员发现,与邻近正常组织相比,TRIM47在HCC组织中表达上调,尤其是在晚期,并且与HCC患者预后不良相关。功能研究表明,TRIM47在体外和体内均能增强HCC细胞的迁移和侵袭能力。机制上,TRIM47通过与SNAI1相互作用,抑制蛋白酶体降解SNAI1,促进HCC转移。总之,本研究揭示了TRIM47在HCC中的促转移作用,揭示了通过CARM1介导的精氨酸甲基化控制TRIM47稳定性的独特机制,并强调了CARM1- crl4crbn -TRIM47- snai1轴在HCC转移中的作用。本研究可能为转移性HCC的治疗提供潜在的治疗靶点。

https://www.nature.com/articles/s41420-024-02244-4
背景知识
01
TRIM家族蛋白是一组E3泛素连接酶。TRIM家族成员参与调节多种生物过程,如自噬、细胞周期、先天免疫反应等。TRIM蛋白的失调与肿瘤发生和肿瘤进展密切相关。TRIM47又称GOA,在非小细胞肺癌(NSCLC)、结直肠癌(CRC)、前列腺癌(PC)等多种肿瘤中表达上调并具有致癌功能。肝细胞癌(HCC)是全球第六大常见癌症和第四大癌症相关死亡原因。一项生物信息学研究报道,TRIM47表达与HCC预后不良相关。基于TRIM家族基因的特征,包括TRIM47和另外5个TRIM基因,在HCC的总生存期(OS)预测中表现良好。这些研究表明TRIM47可能在HCC进展中起重要作用。然而,TRIM47在HCC中的具体作用及其调控机制尚不清楚。
RMT家族由9个成员组成(PRMT1-9),根据其催化活性可分为三组。III型PRMTs仅参与MMA的酶促合成。CARM1是一种I型PRMTs,在许多癌症中不受调控,并通过催化组蛋白或非组蛋白底物蛋白的不对称二甲基化在癌症进展中起关键作用。例如,CARM1通过甲基化染色质重塑因子BAF155促进乳腺癌转移。CARM1对MDH1的精氨酸甲基化抑制谷氨酰胺代谢并抑制胰腺导管腺癌(PDAC)的进展。CARM1通过介导GAPDH的R234甲基化抑制肝癌细胞的糖酵解,从而抑制肝癌细胞的增殖。这与另一项研究相冲突,该研究表明CARM1通过激活AKT/mTOR信号传导促进HCC进展,预示预后不良。这些相互矛盾的结果导致对CARM1在HCC中的功能的理解混乱,因此需要探索其潜在的分子机制。
TRIM47是CARM1的精氨酸甲基化底物
02
研究人员对来自HCC细胞的免疫纯化TRIM47蛋白进行了质谱分析。研究人员为了确定R210和R582是否是TRIM47的主要甲基化位点,将这两个位点突变为赖氨酸(TRIM47R210K或TRIM47R582K),从而抵抗精氨酸甲基化。这些结果表明,R210和R582是TRIM47的主要甲基化位点,即使不是唯一的甲基化位点。此外,TRIM47R210/582K突变体不能与CARM1相互作用。研究人员进一步测试了R210和R582的甲基化是否有助于TRIM47的稳定性和泛素化状态。敲除CARM1后,WT TRIM47的泛素化水平显著提高,而TRIM47R210/582K突变体的泛素化水平几乎没有变化。同样,HY-12759显著降低了WT TRIM47蛋白水平,而TRIM47突变体则没有。研究人员还评估了TRIM47精氨酸突变体对HCC转移的影响。与表达WT TRIM47的细胞相比,表达TRIM47R210K和TRIM47R582K突变体的细胞转移性更低。值得注意的是,TRIM47R210/582K突变体完全消除了TRIM47在HCC中的促转移能力。综上所述,这些数据表明CARM1的甲基化修饰稳定了TRIM47蛋白水平,促进了HCC的转移。
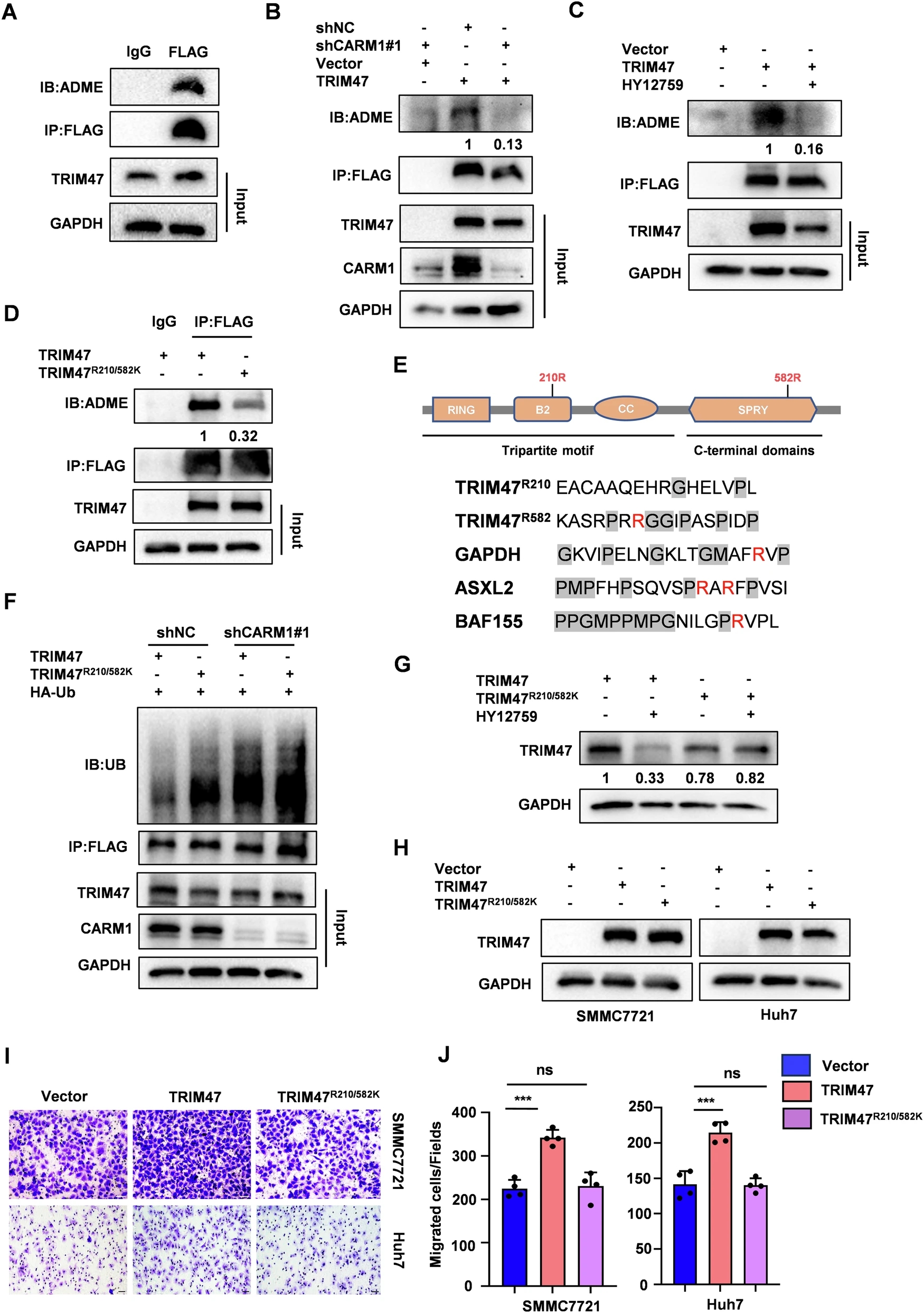
CARM1二甲基化TRIM47的精氨酸210和精氨酸582
TRIM47的甲基化抑制CUL4CRBN对TRIM47的泛素化作用
02
之前的研究表明,CARM1通过抑制TRIM47的泛素化和降解来稳定其蛋白水平。研究人员之前进行的免疫沉淀-质谱联用筛选发现,CRL4 E3泛素连接酶的底物适配体CRBN可能是TRIM47的相互作用蛋白。共定位实验表明,TRIM47确实与CRBN相互作用。CRBN过表达导致TRIM47蛋白水平降低,这一现象可被MG132阻断。同样地,CRBN过表达促进了TRIM47的泛素化。CUL4A过表达也显著增强了TRIM47的泛素化和降解。使用K48或K63位点的泛素突变体(K48或K63)和剩余的赖氨酸被精氨酸替换(K48或K63),研究人员发现CRBN增强了TRIM47的K48位点连接的泛素化。此外,HY15729增强了SMMC7721细胞中CRBN与TRIM47之间的相互作用,导致TRIM47泛素化水平的提高。研究人员进一步研究了CARM1-介导的甲基化是否影响CUL4CRBN调控的TRIM47泛素化。仅过表达CRBN就使WT TRIM47的蛋白水平降低,而TRIM47R2/582A则保持不变。这一新发现揭示了甲基化和泛素化之间的串扰在协调TRIM47蛋白的稳定性。
TRIM47通过保护SNAI1免受蛋白酶体介导的降解而促进HCC转移
03
研究人员接下来探究了CARM1-TRIM47轴抑制HCC转移的潜在机制。研究人员研究了几种影响细胞转移的途径和分子,包括经典WNT/β-连环蛋白信号通路、RhoA/ROCK1信号通路、RAC1通路和上皮间质转化诱导转录因子。有趣的是,只有SNAI1蛋白水平在TRIM47沉默细胞中显著降低。CARM1敲低也抑制了SNAI1蛋白表达。尤其是,共沉淀实验表明SNAI1是TRIM47的结合伴侣。值得注意的是,与CQ相比,MG132治疗可以恢复TRIM47敲低引起的SNAI1蛋白水平降低,这表明TRIM47敲低通过泛素-蛋白酶体途径促进SNAI1降解。为了验证这一点,研究人员进行了蛋白质泛素化分析。TRIM47敲低增强了SNAI1的泛素化。SNAI1过表达完全逆转了TRIM47耗竭对SMMC7721细胞迁移的抑制作用。综合这些结果表明,TRIM47通过保护SNAI1免受蛋白酶介导的降解来促进HCC细胞迁移。
结论
04
总之,研究人员首次发现CARM1-CUL4CRBN-TRIM47-SNAI1级联参与HCC转移。本研究结果强调了TRIM47和CARM1在HCC转移中的作用,揭示了一种新的机制,即精氨酸甲基化和泛素化之间的串扰协调了TRIM47介导的HCC转移。新定义的CARM1-CUL4CRBN-TRIM47-SNAI1调控轴可能为转移性HCC治疗开辟新的途径。(转化医学网360zhyx.com)
【参考资料】
https://www.nature.com/articles/s41420-024-02244-4
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发