【Nature子刊】复旦大学附属肿瘤医院:揭示SHR-1701联合法米替尼在晚期胆道癌和胰管腺癌治疗中的潜力
| 导读 | 团队首次开展了这项II期研究,评估SHR-1701(一种靶向程序性死亡配体1(PD-L1)和转化生长因子-β(TGF-β)的双功能融合蛋白)与法米替尼(一种多靶点受体酪氨酸激酶抑制剂)联合治疗既往标准治疗失败的晚期BTC或PDAC患者的疗效和安全性。 |
2024年12月10日,复旦大学附属肿瘤医院Xie Jing教授团队在期刊《Signal Transduction and Targeted Therapy》上发表了题为“Clinical and biomarker analyses of SHR-1701 combined with famitinib in patients with previously treated advanced biliary tract cancer or pancreatic ductal adenocarcinoma: a phase II trial”的研究论文。探索性分析表明,原发性肿瘤切除史、外周血免疫表型变化和独特的免疫代谢特征与治疗获益相关。团队开发了一种整合了6个基因特征的免疫/代谢评分,作为多个队列中免疫疗法反应的预测性生物标志物,从而筛选出最有可能从这种疗法中获得积极疗效的患者。研究结果提供了概念验证数据,支持SHR-1701加法米替尼作为有效、安全的难治性BTC和PDAC后线疗法的潜力,突出了同时靶向PD-L1、TGF-β和血管生成通路的前景。

https://www.nature.com/articles/s41392-024-02052-3
关于晚期胆道癌
01
SHR-1701是一种新型双功能融合蛋白,由抗PD-L1抗体与TGF-β 受体II的胞外结构域融合而成。与PD1/PD-L1单一疗法相比,SHR-1701在晚期实体瘤(如宫颈癌和胃癌)的初步临床研究中显示出潜在的增强抗肿瘤免疫力的作用。
血管生成是癌症的一个已知特征,因此,它是与免疫疗法相结合的一个有吸引力的干预靶点。法米替尼是一种针对血管内皮生长因子受体2/3、表皮生长因子受体(PDGFR)和c-Kit的多靶点酪氨酸激酶抑制剂(TKI),在与各种恶性肿瘤的ICIs联用时,有望延长无进展生存期(PFS)。
鉴于SHR-1701和法米替尼的互补机制,以及TGF-β激活、免疫耗竭和VEGFA上调之间的重叠特征,团队假设PD-L1、TGF-β和血管生成通路的三重阻断,可能会产生协同抗肿瘤效应并改善患者的临床预后。这项II期试验旨在评估SHR-1701加法米替尼治疗既往标准治疗失败的难治性晚期BTC或PDAC患者的疗效、安全性和潜在的预测性生物标志物。
疗效
02
在BTC患者中,中位反应持续时间(mDoR)为7.6个月,中位PFS(mPFS)为5.1个月。中位OS(mOS)为16.0个月,1年OS率为54.4%,2年OS率为48.1%。BTC组中有7名患者(26.0%)在病情恶化后,接受了后续系统治疗。在PDAC组中,3名获得应答的患者中,1名获得PR,DoR为6.3个月,另外2名获得CR,DoR分别为9.8个月和14个月。14个月生存期的患者死于工作时意外坠楼,与疾病进展无关。mPFS为2.1个月,mOS为5.3个月,1年OS率为39.6%。PDAC队列中有4名患者(16.7%)在病情恶化后,接受了后续系统治疗。
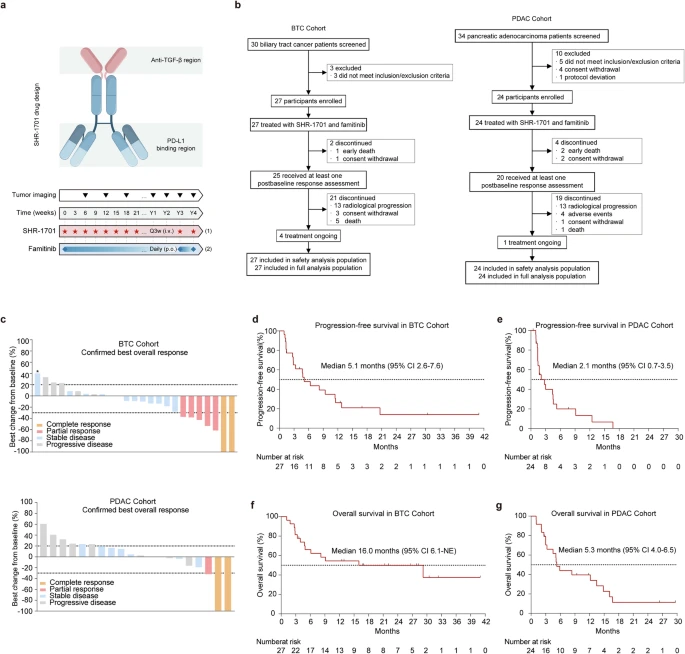
SHR-1701联合法米替尼治疗晚期BTC和PDAC的研究设计和临床结果。
安全性
03
大多数患者(88.2%)至少出现过1次治疗相关不良事件(TRAE)。最常见的不良事件是蛋白尿(47.1%)、贫血(39.2%)和尿潜血阳性。15例患者(29.4%)出现了3级或4级TRAE,其中最常见的是贫血(13.7%)和高血压(7.8%)。此外,16例患者(31.4%)出现了潜在的免疫相关不良事件,最常见的是皮疹(23.5%)和甲状腺功能减退(13.7%)。其中,2例(3.9%)为3-4级。共有8名受试者接受了免疫抑制治疗,其中4例因皮肤毒性而外用皮质类固醇激素。未报告5级TRAE。
分别有7例(13.7%)和8例(15.7%)患者因TRAE导致SHR-1701治疗中断和停药。至于法米替尼,TRAEs导致17例(33.3%)治疗中断,11例(21.6%)剂量减少,5例(9.8%)治疗中止。总体而言,有4例患者(7.8%)因TRAEs而中断了所有治疗。
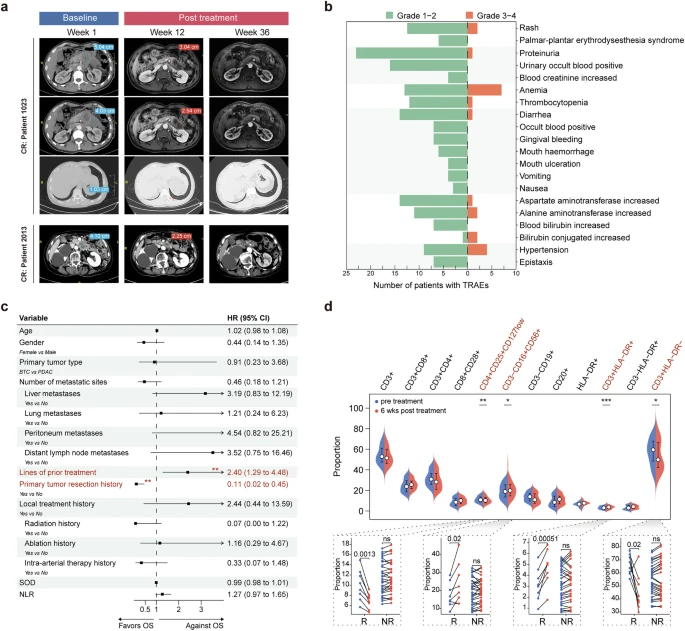
研究的安全性概况和临床病理参数分析。
总结
04
1. 治疗效果:SHR-1701联合法米替尼在既往治疗失败的晚期BTC或PDAC患者中显示出良好的疗效,BTC队列的客观反应率(ORR)为28%,PDAC队列的ORR为15%,完全反应(CR)率分别为8%和10%。BTC患者的中位总生存期(OS)为16.0个月,PDAC患者的中位生存期为5.3个月。
2. 与其他疗法比较:与Lenvatinib和pembrolizumab治疗晚期BTC患者的ORR(10%)和中位OS(8.6个月)相比,SHR-1701联合法米替尼显示出更好的疗效。
3. 药物组合策略:将双特异性抗体与抗血管生成药物配对使用,可以为免疫介导的肿瘤破坏创造更有利的微环境,提高疗效。
4. 安全性:SHR-1701联合法米替尼的安全性可控,最常见的治疗相关不良事件(TRAE),包括蛋白尿、贫血和尿潜血阳性。
5. 预后相关因素:一些基线特征与预后相关,如先期原发肿瘤切除术是改善OS的关键因素。
6. 生物标志物分析:较低的CEA或CA 19-9基线水平以及外周血免疫表型的变化,与治疗效果的改善相关。
7. 耐药机制:应答者表现出较高水平的TGF-β和血管生成途径,支持SHR-1701和法米替尼联合用药的合理性。
8. 未来方向:需要在更大规模的前瞻性临床试验中验证这些发现,并探索新的治疗靶点。
参考资料:
1.Siegel, R. L., Miller, K. D., Wagle, N. S. & Jemal, A. Cancer statistics, 2023. CA Cancer J. Clin. 73, 17–48 (2023).
2.Rizzo, A. & Brandi, G. Pitfalls, challenges, and updates in adjuvant systemic treatment for resected biliary tract cancer. Expert Rev. Gastroenterol. Hepatol. 15, 547–554 (2021).
 腾讯登录
腾讯登录






还没有人评论,赶快抢个沙发