【Nature子刊】上海市胸科医院陆舜团队:免疫检查点抑制剂疗效的无创早期识别
| 导读 | 研究结果表明,整合ctDNA的早期变化、正常化的bTMB和首次RECIST反应可以准确、无创、及早地预测接受ICIs治疗的NSCLC患者的持久获益。 |
2024年12月16日,上海交通大学附属胸科医院肿瘤科陆舜教授团队在期刊《Signal Transduction and Targeted Therapy》上发表了题为“Noninvasive early identification of durable clinical benefit from immune checkpoint inhibition: a prospective multicenter study (NCT04566432)”的研究论文。研究结果表明,整合ctDNA的早期变化、正常化的bTMB和首次RECIST反应可以准确、无创、及早地预测接受ICIs治疗的NSCLC患者的持久获益。科学界有必要进一步开展前瞻性研究,以验证这些发现并指导临床决策,为NSCLC患者提供最佳免疫疗法。

https://www.nature.com/articles/s41392-024-02060-3
关于非小细胞肺癌
01
阻断抑制性程序性死亡配体 1(PD-L1)或程序性细胞死亡1受体(PD-1)的免疫检查点抑制剂(ICIs)彻底改变了癌症疗法,为各类恶性肿瘤患者带来了新的希望。这种反应的差异性凸显了对可靠的预测性生物标志物的迫切需求,以对可能从ICI治疗中获益的患者进行分层。
2020年10月,Nabet等人开发出一种出色的无创多参数检测方法 (DIREct-On),用于预测可获得持久临床获益(DCB,超过6个月)的患者。在DIREct-On模型中整合了治疗前ctDNA、外周CD8 T细胞水平和早期ctDNA动态。受DIREct-On研究的启发,团队设计了这项多中心前瞻性观察临床试验,以探索在临床常规中预测非EGFR/ALK NSCLC患者ICI治疗DCB更为可行的多模态模型。团队整合了治疗前和治疗早期血液样本中的ctDNA图谱数据(包括bTMB、VAF或ctDNA浓度)、治疗前血液样本中的循环免疫细胞,以及早期放射学反应来开发模型。团队还将已发表的DIREct-On研究作为独立的外部验证队列,来验证该模型。这种方法有望改善患者预后,减少不必要的治疗费用和副作用。
早期影像学RECIST反应可预测DCB,特异性高但敏感性低
02
共有75例患者进行了早期影像学RECIST反应评估(ICI治疗后2个月内,主要是2个ICI治疗周期后),其中分别有25例、43例和7例患者获得了部分反应(PR)、疾病稳定(SD)和疾病进展(PD)。获得RECIST反应的患者的PFS,比未获得反应的患者长。然而,早期成像RECIST反应预测DCB的敏感性为41.5%,特异性为86.4%,预测准确性为54.7%。被归类为ctDNA分子反应者的患者的PFS,长于非反应者(中位PFS:9.8个月 vs 5.8个月。
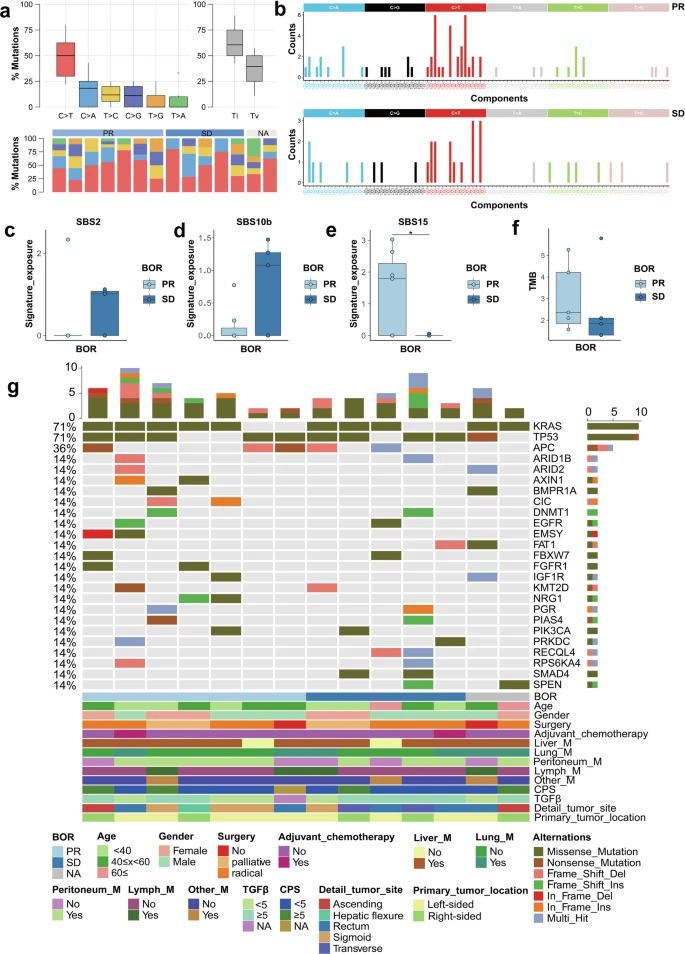
早期成像RECIST评估,可预测对ICI的反应。
预测ICI反应的多模式模型
03
该模型能够预测DCB,AUC为0.854,灵敏度为75.0%(分类DCB),特异度为88.9%(准确率=79.5%)。此外,该模型在验证队列中也有类似的表现,AUC为0.798,灵敏度为80.5%,特异度为67.6%(准确率=74.7%)。该模型的预测性能明显优于每个单独指标。预测得分较高的患者,生存期大大长于预测得分较低的患者(训练队列:中位生存期为13.6个月 vs 4.3个月;验证队列:中位生存期为8.5个月 vs 2.5个月)。
在训练队列中,加入RECIST反应后,模型灵敏度从75.0%提高到79.2%,但特异度却从88.9%降至86.4%。然而,在验证队列中,灵敏度(从80.5%提高到94.7%)和特异性(从67.6%提高到85.3%)都得到了提高。
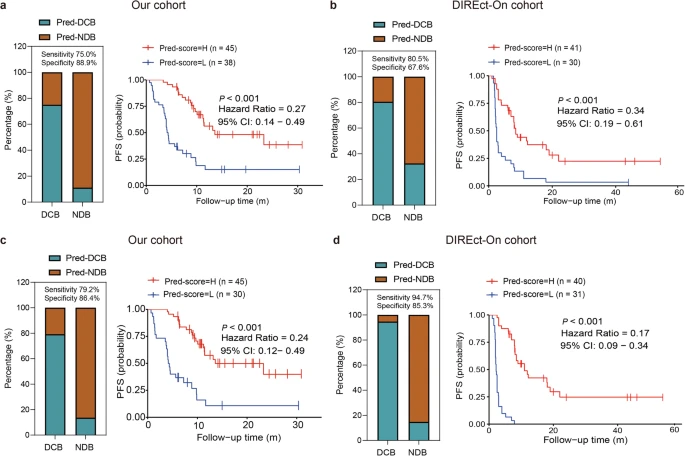
多模态模型可实现完全无创的结果分类。
总结
04
1. DIREct-On模型验证:在DIREct-On研究的独立队列中验证了该模型,显示治疗前CD8 T细胞水平可分类DCB或NDB患者,准确率为70%。
2. 循环CD8 T细胞和NK细胞差异:循环CD8 T细胞水平在ICI应答者和非应答者间无显著差异,而基线循环活化NK细胞水平较低的患者往往在ICI后有较长的无进展生存期(PFS)。
3. ctDNA变化与ICI反应:治疗开始后1-4个周期的ctDNA变化可以对NSCLC的ICI反应进行分类,但准确率不高。
4. 模型性能:首次成像评估的高特异性提高了模型的性能,有助于区分假性进展人群和最终无法获得DCB的SD患者。
5. 未来方向:需要进一步开展前瞻性干预研究,以验证该模型在指导NSCLC患者最佳免疫疗法临床决策方面的有效性。
参考资料:
1.Reck, M. et al. Pembrolizumab versus chemotherapy for PD-L1-positive non-small-cell lung cancer. N. Engl. J. Med. 375, 1823–1833 (2016).
2.Gandhi, L. et al. Pembrolizumab plus chemotherapy in metastatic non-small-cell lung cancer. N. Engl. J. Med. 378, 2078–2092 (2018).
 腾讯登录
腾讯登录




还没有人评论,赶快抢个沙发