【Nature子刊】抗癌新希望:美国贝勒医学院开发RIPK1降解剂,显著提升肿瘤免疫反应
| 导读 | 为了应对RIPK1中间结构域内一个定义不清的结合口袋所带来的挑战,团队利用蛋白水解靶向嵌合体(PROTAC)技术开发了一种RIPK1降解剂 LD4172。 |
2024年12月16日,美国贝勒医学院Wang Jin教授团队在期刊《Nature Communications》上发表了题为“Development of a RIPK1 degrader to enhance antitumor immunity”的研究论文。研究结果表明,LD4172在体外和体内都表现出强效和选择性的RIPK1降解作用。LD4172降解RIPK1会引发免疫性细胞死亡,增强肿瘤浸润淋巴细胞反应,并使雌性C57BL/6J小鼠的肿瘤对抗PD1疗法敏感。

https://www.nature.com/articles/s41467-024-55006-2
关于RIPK1抑制剂
01
受体相互作用蛋白激酶1(RIPK1)通过其依赖和不依赖激酶的功能调节细胞命运,并控制多种先天性免疫通路下游的促炎反应,包括由肿瘤坏死因子-α(TNF-α)、收费样受体配体和干扰素(IFNs)引发的反应。最近的研究表明,基因敲除RIPK1,而非其激酶结构域失活,可使B16F10肿瘤对ICBs敏感。因此,靶向RIPK1支架功能,有望成为与ICBs协同促进抗肿瘤免疫的一种策略。
迄今为止开发的所有RIPK1抑制剂都侧重于抑制激酶功能,以治疗自身免疫性疾病、炎症性疾病和神经退行性疾病,但由于RIPK1中间结构域内缺乏定义明确的结合口袋,因此,开发特异性靶向RIPK1中间结构域的抑制剂仍具有挑战性。蛋白水解靶向嵌合体(PROTAC)是一种异功能分子,它能同时结合靶蛋白和E3泛素连接酶,促进三元复合物的形成,导致靶蛋白泛素化并最终降解。
LD4172使肿瘤对抗PD1治疗敏感
02
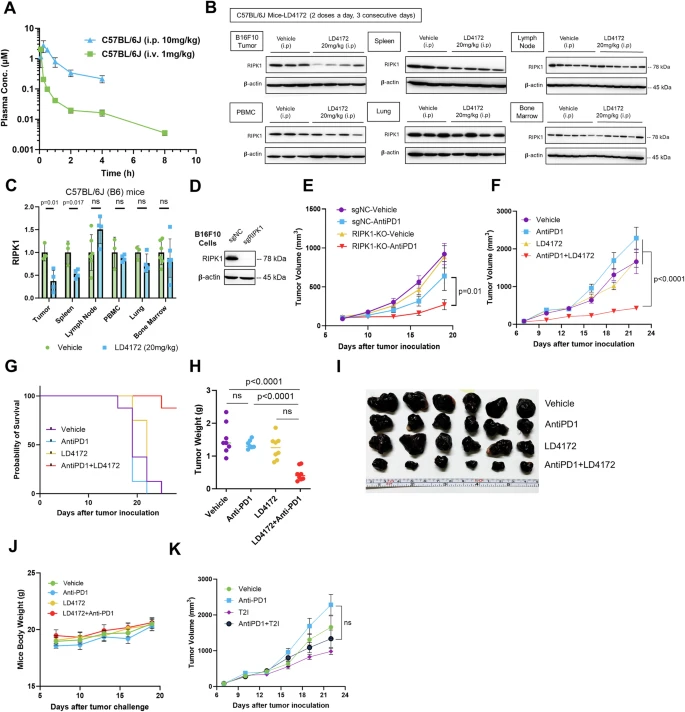
LD4172与抗-PD1协同抑制肿瘤生长。
LD4172增强抗肿瘤免疫力
03
LD4172和抗-PD1联合疗法显著增强了免疫冷冻B16F10肿瘤的抗-PD1阳性,表现为CD8+T细胞浸润增加,TME内FOXP3+T调节细胞浸润减少。在CD8+T细胞缺失的情况下,抗PD1和LD4172的协同作用无效。血浆细胞因子阵列分析的结果进一步证实了联合治疗的协同效应,显示免疫细胞增殖细胞因子,包括IFN-γ和IL2的产生显著增强。

LD4172可改变肿瘤免疫微环境。
总结
04
1. RIPK1的作用与挑战:RIPK1是一个关键的调节因子,参与细胞过程和促炎信号转导,与癌症免疫疗法的抗性有关,但因缺乏明确的结合口袋,开发针对其中间支架结构域的抑制剂具有挑战性。
2. PROTAC技术的应用:利用PROTAC技术开发的RIPK1降解剂LD4172,能在体外和体内有效且特异性地降解RIPK1。
3. RIPK1在TNF-α信号传导中的作用:RIPK1在TNF-α信号传导中充当重要支架,LD4172诱导的RIPK1降解显著影响NF-κB激活,与TNF-α联合作用可诱导细胞凋亡。
4. LD4172的抗肿瘤效果:LD4172能诱导肿瘤内RIPK1降解,与抗PD1治疗联合使用时,显示出抑制肿瘤生长的协同效应。
5. 免疫原性通路的激活:降解RIPK1作为免疫原性通路的制动器,需要额外配体来完全激活这些途径,抗-PD1可通过促进TNF的产生提供这些配体。
6. 肿瘤免疫微环境的重塑:LD4172与抗-PD1联用时,可通过增强树突状细胞和IFNγ+T细胞的浸润,以及促进免疫刺激细胞因子的分泌,来重塑肿瘤免疫微环境。
7. RIPK1降解剂的靶向毒性特征:RIPK1降解剂的安全性和组织特异性降解,需要在未来的临床研究中进行评估。
8. RIPK1降解剂的潜在优势:RIPK1降解剂有可能改善癌症免疫疗法,其药理降解与抗PD1协同作用,可克服对ICB的耐药性。
9. 肿瘤选择性RIPK1降解:LD4172可能利用肿瘤中白蛋白的积累,实现肿瘤选择性降解RIPK1,减轻与正常组织中RIPK1降解有关的潜在毒性问题。
参考资料:
1.Korman, A. J., Garrett-Thomson, S. C. & Lonberg, N. The foundations of immune checkpoint blockade and the ipilimumab approval decennial. Nat. Rev. Drug Discov. 21, 509–528 (2022).
2.Vesely, M. D., Zhang, T. & Chen, L. Resistance mechanisms to anti-PD cancer immunotherapy. Annu. Rev. Immunol. 40, 45–74 (2022).
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发