澳大利亚纽卡斯尔大学:DNA复制应激或成结直肠癌治疗的“金钥匙”
| 导读 | 在这项研究中,团队发现抑制OXPHOS同样能抑制体外和源自患者的CRC异种移植中具有糖酵解能力的结直肠癌(CRC)细胞的增殖和致瘤性。 |
2025年1月14日,澳大利亚纽卡斯尔大学张旭东教授、金雷博士团队在期刊《Cell Death & Disease》上发表了题为“DNA replication stress underpins the vulnerability to oxidative phosphorylation inhibition in colorectal cancer”的研究论文。研究结果表明,GOT1靶向是使癌细胞对OXPHOS抑制剂敏感的潜在途径,从而降低有效抑制癌症生长所需的剂量,同时减轻抑制剂的不良反应。

https://www.nature.com/articles/s41419-025-07334-4
关于结直肠癌
01
在临床前研究中,线粒体复合体I抑制剂能有效抑制癌细胞的增殖,但不诱导细胞死亡。然而,在有糖酵解能力的癌细胞中靶向OXPHOS的表型和机理后果,仍然不太清楚。靶向OXPHOS也可能对具有糖酵解能力的癌症有效。
在这项研究中,团队证明了靶向OXPHOS能抑制糖酵解功能健全的CRC细胞的增殖和致瘤性,这与糖酵解功能缺陷的癌细胞类似。靶向OXPHOS有可能有效治疗CRC和其他具有糖酵解能力的癌症类型,而抑制GOT1是使CRC细胞对OXPHOS靶向疗法敏感的一种潜在方法。
靶向GOT1可使有糖酵解能力的CRC对OXPHOS抑制敏感
02
与单独治疗相比,联合治疗有效抑制了Colo205-shGOT1异种移植物的生长,同时Ki67阳性细胞的比例进一步下降)。此外,从联合使用Dox和IACS-010759治疗的小鼠体内分离出的CRC细胞,显示出天冬氨酸水平的进一步降低。停止Dox治疗后,GOT1的表达恢复,肿瘤生长也得以恢复,这表明生长变化与GOT1的水平有关。
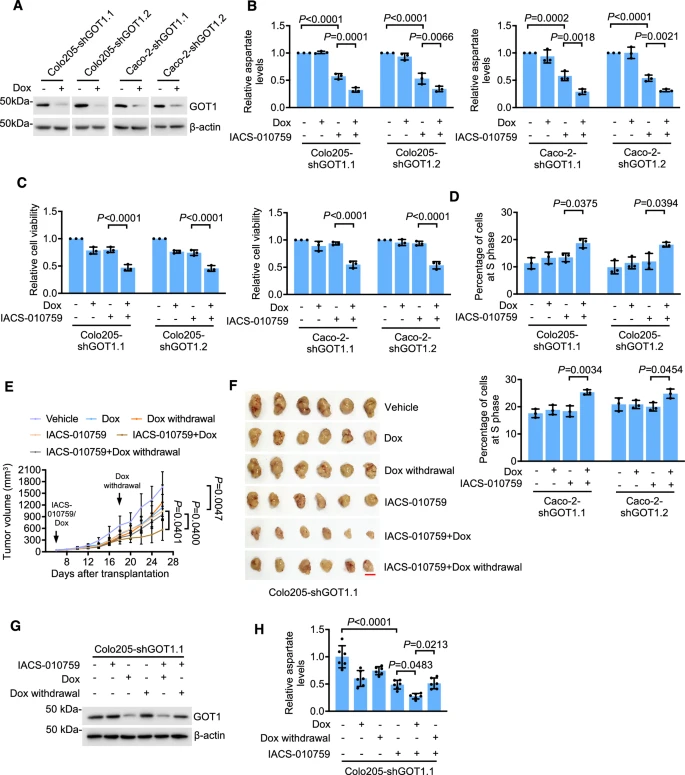
靶向GOT1可使具有糖酵解能力的CRC细胞对OXPHOS抑制作用敏感。
总结
03
1. 研究显示,在体外和临床前PDX CRC模型中,具有糖酵解能力的CRC细胞易受靶向OXPHOS的影响,且GOT1在保护CRC细胞免受OXPHOS抑制方面发挥重要作用,可作为提高OXPHOS抑制剂疗效的潜在策略。
2. 在有糖酵解能力的CRC细胞中,靶向OXPHOS未显著降低细胞ATP水平,但会导致细胞周期停滞在S期、复制叉减慢和p53通路激活,这些机制由天冬氨酸短缺导致的核苷酸不足引起。
3. 携带野生型p53的糖酵解能力强的CRC细胞比携带突变型p53的细胞对IACS-010759更敏感,但这种差异在克隆形成实验中减小,表明p53信号转导以外的机制在决定CRC细胞命运时也很重要。
4. p53的敲除减轻了IACS-010759诱导的复制叉停滞和增殖抑制,且野生型和突变型p53 CRC细胞经IACS-010759处理后天门冬氨酸水平降低程度无明显差异,表明靶向OXPHOS可抑制CRC细胞的天门冬氨酸生物合成,与细胞的p53状态无关。
5. 研究未发现IACS-010759处理后CRC细胞中mtDNA复制和分布、线粒体形态有显著变化,表明OXPHOS抑制不会导致mtDNA应激或改变线粒体动力学。
6. 通过靶向GOT1抑制细胞膜天冬氨酸的生物合成,可使有糖酵解能力的CRC对OXPHOS抑制剂敏感;GOT1和IACS-010759的组合可降低有效抑制CRC生长所需的浓度,减轻剂量限制毒性,随着GOT1特异性抑制剂的开发,其组合有望在临床前模型中进一步研究。
参考资料:
1.DeBerardinis RJ, Chandel NS. Fundamentals of cancer metabolism. Sci Adv. 2016;2:e1600200.
2.Xu Y, Xue D, Bankhead A 3rd, Neamati N. Why all the fuss about oxidative phosphorylation (OXPHOS)? J Med Chem. 2020;63:14276–307.
 腾讯登录
腾讯登录






还没有人评论,赶快抢个沙发