调控肝癌细胞生长并影响肝细胞分化!浙江大学研究团队:有前景的肝癌治疗靶点
| 导读 | RNA 聚合酶 II 相关蛋白 2(RPAP2)在转录调控中发挥着关键作用。然而,关于 RPAP2 是否以及如何调节肝细胞癌(HCC)细胞生长,以及 RPAP2 的稳定性是如何被精确维持的,人们知之甚少。 |
2月11日,浙江大学研究团队在期刊《Advanced Science》上发表了研究论文,题为“The FBXW7-RPAP2 Axis Controls the Growth of Hepatocellular Carcinoma Cells and Determines the Fate of Liver Cell Differentiation”,本研究中,研究人员发现在肝细胞癌(HCC)组织中,高 RPAP2 水平与患者生存率低相关。RPAP2 耗竭会抑制 HCC 细胞的生长和存活。HSP90 抑制显著促进 CRL5FBXW7 连接酶介导的 RPAP2 降解,而 USP7 则去泛素化并稳定 RPAP2。FBXW7 敲低通过体外和体内积累 RPAP2 促进 HCC 细胞生长。综上所述,本研究证明了 RPAP2 的稳定性受 FBXW7 负调控,但受 HSP90 和 USP7 正调控。FBXW7-RPAP2 轴调节 HCC 细胞生长并影响肝细胞分化命运。这些发现为致癌 RPAP2 可能成为 HCC 的有前景的治疗靶点提供了证据。

https://advanced.onlinelibrary.wiley.com/doi/full/10.1002/advs.202404718
在真核生物中,RNA 聚合酶 II(RNAPII)在蛋白质编码基因以及大多数小核 RNA 基因的转录过程中发挥着关键作用。RNA 聚合酶 II 的 B1 亚基(RPB1)是 RNAPII 中最大的亚基,其羧基末端结构域(CTD)由多个重复的共识序列 Tyr1-Ser2-Pro3-Thr4-Ser5-Pro6-Ser7 组成,并在整个转录周期中经历可逆的磷酸化。CTD 的动态磷酸化由多种激酶和磷酸酶调节,影响转录和共转录过程中的多个关键步骤,包括预起始复合物的组装、启动子近端暂停、延伸、终止和 RNA 加工。
RNA 聚合酶 II 相关蛋白 2(RPAP2)是酵母转录调节因子 1(Rtr1)的人类同源物,最初是通过与 RNA 聚合酶 II 共纯化而被发现的,并且被发现参与其核输入。后续研究表明,RPAP2 的耗竭会增加 CTD 中的 Ser5 磷酸化,表明其磷酸酶活性对该残基具有特异性。然而,结构研究和体外磷酸酶测定表明,具有非典型磷酸转移结构域的 RPAP2 表现出低或检测不到的磷酸酶活性。尽管最近大多数研究都集中在 RPAP2 的转录调节功能上,包括转录起始和终止,但其在调节其他生物过程中的作用,尤其是肝肿瘤生长方面,仍知之甚少。此外,负责调节 RPAP2 稳定性的上游信号通路尚不清楚。
泛素 - 蛋白酶体系统对于维持细胞内稳态至关重要,它通过调节参与各种生物过程的多个关键成分的稳定性来发挥作用。这些成分由 E3 泛素连接酶标记上多个泛素分子,从而被泛素 - 蛋白酶体系统降解,而这一过程可被去泛素化酶逆转。因此,E3 泛素连接酶和去泛素化酶协同作用以维持蛋白质稳态,而这种协调的失衡会导致包括癌症在内的多种人类疾病。
RPAP2 基因沉默抑制体外和体内肝癌细胞的生长
01
肝细胞癌(HCC)组织中 RPAP2 水平升高表明其在生长调控中发挥作用。为验证这一可能性,研究人员首先敲低 RPAP2,然后进行了基于细胞计数试剂盒 8(CCK8)的细胞生长测定。RPAP2 敲低显著抑制了 Huh7、Hep3B 和 PLC/PRF/5 细胞的生长。此外,克隆形成存活实验表明,RPAP2 沉默显著抑制细胞存活,表现为 Huh7、Hep3B 和 PLC/PRF/5 细胞形成的克隆数量减少。相反,稳定过表达 RPAP2 的 Huh7 细胞表现出增强的生长,并形成了比模拟对照细胞更多的克隆。鉴于 mTOR 在促进肿瘤发生方面的作用已得到充分证实,这些结果表明 RPAP2 通过调节 mTOR 通路促进细胞生长和存活。此外,流式细胞术分析显示,RPAP2 沉默显著诱导 Huh7 和 HeLa 细胞的 G1 期阻滞。免疫印迹法持续表明,RPAP2 基因沉默会导致 G1/S 检查点的两种著名细胞周期蛋白依赖性激酶抑制剂 p21 和 p27 的水平升高。这些数据表明,RPAP2 通过促进细胞周期进程来调控肝癌细胞的生长。尤其是,无论是通过敲低还是过表达来改变 RPAP2 的水平,对正常肝细胞 L02 的生长和存活都没有显著影响,这表明 RPAP2 调控肝癌细胞的生长而不影响正常肝细胞。
为了进一步探究 RPAP2 是否促进肝细胞癌(HCC)细胞在体内的生长,研究人员使用了异种移植小鼠模型,发现通过慢病毒 shRNA 介导的 RPAP2 敲低几乎完全抑制了 Huh7 和 Hep3B 细胞在体内的生长,这从肿瘤体积和重量的减少中得到了证实。相反,在 Huh7 细胞中过表达 RPAP2 与对照细胞相比,导致了更大的肿瘤。此外,RPAP2 的缺失或过表达并未诱导细胞毒性,这从用于异种移植实验的细胞中γH2AX 和 TUNEL 染色呈阴性得到了证明。阳性对照显示,VP16 处理的细胞中γH2AX 染色显著,DNase I 处理的细胞中 TUNEL 染色强烈。综上所述,这些结果表明 RPAP2 促进 HCC 细胞在体内的生长。
鉴于 RPAP2 在肝细胞癌(HCC)细胞中的促生长作用,研究人员接下来确定了 RPAP2 蛋白水平是否与 HCC 细胞对 17-AAG 的敏感性相关。为此,研究人员首先检测了多个 HCC 细胞系中 RPAP2 的水平,发现 Huh7 和 JHH7 细胞中 RPAP2 蛋白水平较高,Hep3B 和 PLC/PRF/5 细胞中水平较低,而 SNU-423 细胞中几乎检测不到。接下来,研究人员在八个 HCC 细胞系中确定了对 HSP90 抑制剂敏感性与 RPAP2 水平之间的相关性。异位表达 RPAP2 使 SNU-423 细胞对 HSP90 抑制剂敏感,导致 17-AAG 的 IC50 值从 10.14 降至 6.25 微米。这种敏感性增强是由于 17-AAG 诱导的细胞凋亡增强所致,这从 PARP 和 Caspase-3 的裂解增加得到了证实。研究结果表明,RPAP2 水平与对 HSP90 抑制剂的敏感性相关,这表明 RPAP2 可能作为 HSP90 靶向治疗的潜在生物标志物。(转化医学网360zhyx.com)
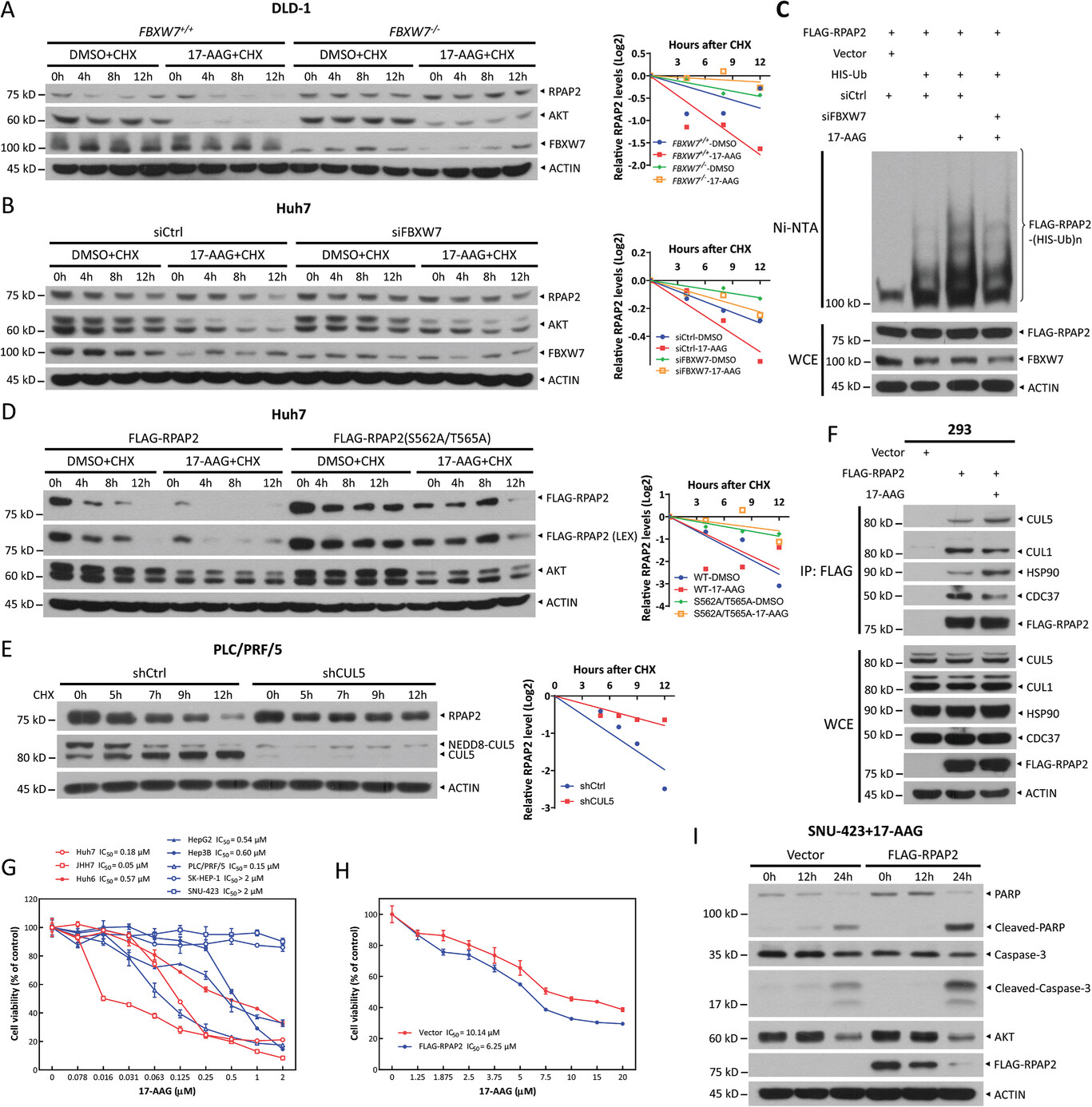
HSP90 抑制剂诱导 RPAP2 通过 FBXW7 和 CUL5 介导的降解
【参考资料】
https://advanced.onlinelibrary.wiley.com/doi/full/10.1002/advs.202404718
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发