敌人的敌人就是朋友,化敌为友,肿瘤治疗新方法
| 导读 | 肿瘤的治疗一直是火热的话题。在过去的50年中,通过对恶性肿瘤的规范化治疗,癌症患者的预后得到了显着改善,但放眼全球,但癌症仍然是死亡的主要原因。肿瘤复发、肿瘤转移和肿瘤微环境(TME)仍然是妨碍临床癌症治疗的三个未完全解决的关键问题。 |
肿瘤的治疗一直是火热的话题。在过去的50年中,通过对恶性肿瘤的规范化治疗,癌症患者的预后得到了显着改善,但放眼全球,但癌症仍然是死亡的主要原因。肿瘤复发、肿瘤转移和肿瘤微环境(TME)仍然是妨碍临床癌症治疗的三个未完全解决的关键问题。
目前以癌症为中心的治疗方法(比如传统的放疗及化疗等),通常不能完全根除恶性肿瘤,因为肿瘤基质可能促使肿瘤复发,并且对治疗产生抵抗。肿瘤基质细胞就是肿瘤生存的微环境(TME),在肿瘤基质细胞中,癌症相关成纤维细胞(CAF)是最丰富的,并且研究证实CAF与癌症进展密切相关。CAF通过细胞-细胞接触释放,来调节肿瘤细胞和其他基质细胞的生物学行为,影响许多调节因子的合成、甚至重塑细胞外基质,因此这些细胞可影响肿瘤的发生和发展。
人体与癌症的关系就如同土壤与种子的关系。植物的生长要靠肥沃的土地、充足的水分、优良的种子,如果土壤与种子等各种条件都非常适宜,那么就茁壮成长,否则,土壤好种子不好,当然生长不好,土壤不好再是优良品种也没有用,最后还是不能茁壮成长。人体内癌细胞之所以生长并扩散转移,四处生根发芽,少不了肥沃土壤的帮助。

如果把每个肿瘤细胞都看成是一粒种子,那么TME(肿瘤微环境)就是培养种子的土壤,它可以创造肿瘤的“壁垒”,保护肿瘤细胞免受治疗的攻击,导致治疗失败。
研究得知,TME是具有复杂肿瘤-基质相互作用的多细胞系统,癌症相关成纤维细胞(CAF)是TME中含量最丰富的基质成分之一,是培育优质土壤的主要幕后黑手。大量研究表明,CAF在癌症发病机制中具有重要作用。
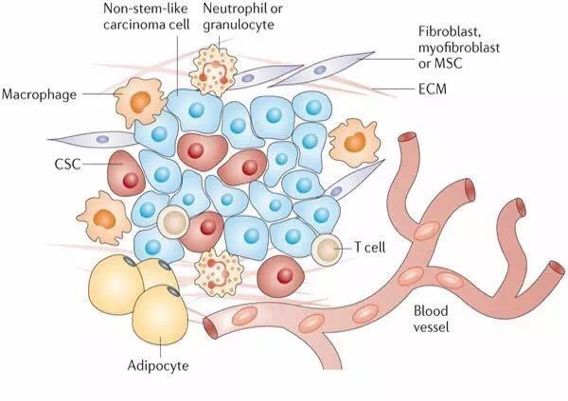
在具体机制上,癌症相关成纤维细胞(CAF)可构建并重塑细胞外基质结构,使肿瘤细胞能够通过肿瘤微环境(TME)侵犯外围正常细胞。
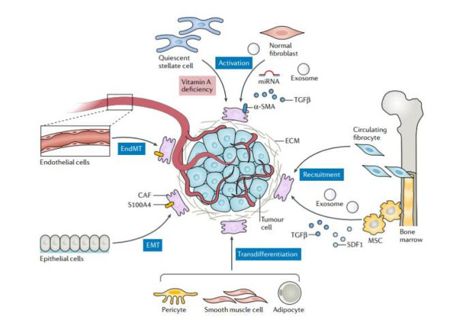
癌症相关成纤维细胞(CAF)还分泌大量生长因子和促炎细胞因子和趋化因子,特别是转化生长因子-β(TGFβ),白细胞介素-6(IL-6)和CC-趋化因子配体2(CCL2),不仅可以加速肿瘤细胞生长,还能募集免疫细胞进入肿瘤基质,以协助免疫逃避,促进肿瘤扩散和转移。
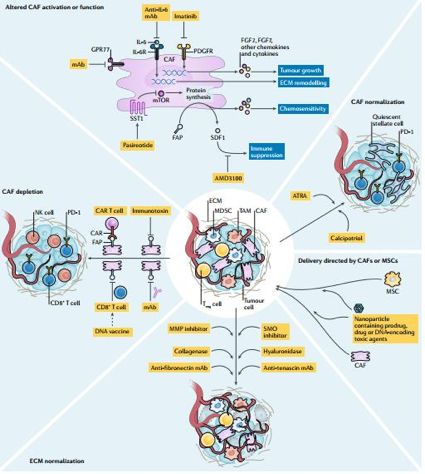
总体而言,癌症相关成纤维细胞(CAF)通过产生多种ECM蛋白和调节因子在构建有利于肿瘤发生、血管生成、肿瘤转移的微环境中发挥关键作用。所以在过去,科学家们一味的认为CAF在肿瘤发生、发展及转移过程中起到推波助澜的作用,所以以往的肿瘤治疗方法,当然是将他们赶尽杀绝。
但是时过境迁,科技是进步的,事物不是一成不变的,昔日的止痛片、降糖药或可进行抗癌治疗,就连四处助纣为虐的CAF,神奇的化敌为友,也变成了人类抵御癌症的好帮手。
近日《NATURE》子刊发文,基于CAF的表征研究,科学家们在CAF家族中发现一些亚群,被证实可以抑制肿瘤的生长,美国科学家Brechbuhl, H. M 报道乳腺癌TME中具有至少两个可通过CD146表达区分的CAF亚组,CD146 + CAF增加雌激素依赖性及管腔乳腺癌细胞对他莫昔芬的敏感性,而CD146-CAF抑制雌激素受体表达和癌细胞对雌激素的反应性,导致肿瘤对他莫昔芬产生药物抗性。基于此特性,科学家认为肿瘤抑制性CAFs具有治疗癌症的潜力。将其靶向细胞疗法或与免疫药物结合使用,是一个新的研究方向。
以往癌症治疗过程中用于整个CAF群体的非选择性治疗(即不分敌我)可能是无效的,甚至是有害的。举一个非常简单的例子,人类使用抗生素治疗细菌感染,但是同时也会杀死体内的益生菌,造成菌群失调,引发其他疾病。所以说,需要区分促肿瘤CAF亚群和肿瘤抑制性CAF亚群,找出靶点,以用于精准靶向治疗。 因此,科学家们通过更具体和可靠的细胞表面标志物,以区分促肿瘤CAF和抗肿瘤CAF,以便将来进行精确治疗。
精准靶向CAF治疗联合其他治疗如免疫治疗,不仅可以抑制癌症“种子”,还可以改变孕育肿瘤细胞的“土壤”,以构建抑制肿瘤生长的微环境,把癌症相关成纤维细胞(CAF)从促使肿瘤生长的“敌人”变成抑制肿瘤生长或转移的“朋友”。
参考文献:
1.Turning foes to friends: targeting cancer- associated fibroblasts
2.This is a systematic Review on the biology and function of fibroblasts in cancer.
3.This study provides the first evidence for different CAF subsets with diverse biological functions, defined by cell surface markers, and is the first time that a tumour- promoting CAF subset was selectively targeted in an animal tumour model.
4.This is the first report that provides precise characterization of CAF heterogeneity in cancer
5.This is a comprehensive Review of tumourassociated MSCs as cancer therapeutic targets.
6.Fibroblast subtypes regulateresponsiveness of luminal breast cancer to estrogen
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发